SUV 的困局
2020-12-24 来源:西门子
SUV 的困局
原创Alexandra MI V CLUB
SUV
想说爱你不容易
Aide教授开篇介绍了SUV值的准确性受非常多的因素影响[2]。简单概括一下包括:技术因素、生理因素和物理因素三个方面。正是由于SUV受如此多不同因素的影响,即使每一个因素只有微小影响,累加起来会造成SUV值的巨大差异。特别是近年来,伴随着图像重建算法的不断创新,不同重建算法之间所带来的SUV差异也呈现倍数级的差异。所以,SUV值的标准化、均一化就显得尤为重要。

由于体重对SUV值有决定性的影响,Aide教授的团队进行了两年多的研究,发现PET申请单上的患者体重、患者口述的自身体重与患者的实际体重具有巨大的差异,而这一因素是影响SUV值、甚至患者疗效评估结果的重要而又简单的原因。
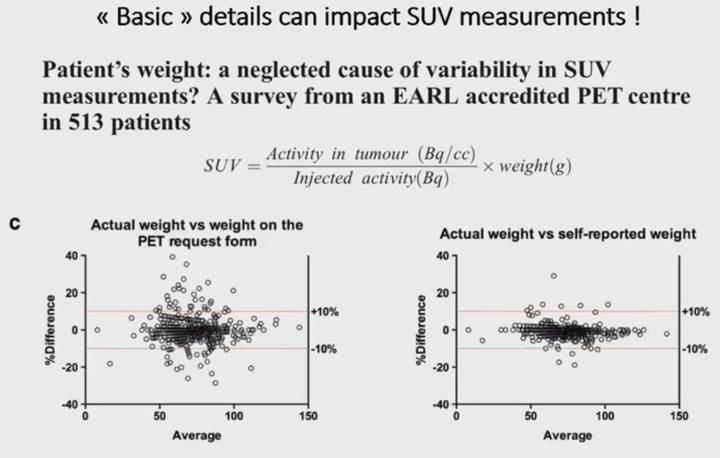
为了实现SUV测量的可比性,欧洲European Association Research Ltd (EARL) [3]和北美Quantitative Imaging Biomarker Alliance (QIBA) [4]分别推出了相应的SUV定量分析标准,对患者准备、图像采集和重建做出了统一标准。


其中对于重建参数的相关变量,EARL认证并推荐了一种SUV均一化方案,即通过引入高斯滤波参数的方法对重建图像进行均一化处理[5],进而得到SUV均一化的图像。这一方案包含两次图像重建:
1.使用每家医院、每台设备各自适用的重建方法,获得优化的重建图像,以达到最佳的诊断效果。
2.通过NEMA测试计算该设备对应重建方法下的活度恢复系数,并得出符合SUV均一化标准的滤波参数,在重建算法中引入均一化滤波参数,获得均一化的重建图像,实现SUV测量的可重复性。
经研究证实,这一方案能够很好的实现SUV的均一化,将SUV测量的差异减少近4倍,极大的提升了SUV在临床诊断中的应用价值。当然,这种重建两次的方案给医生带来了新的工作负担。
SUV恒准定量
2015年,英国牛津大学与西门子共同研发的EQ.PET问世解决了这一临床难题。通过数据集的整合,使用EQ.PET,医生只需要输入均一化滤波参数(EQ Filter),就可以一键同时获取优化的诊断图像和均一化的定量数据,大大的简化了操作流程。
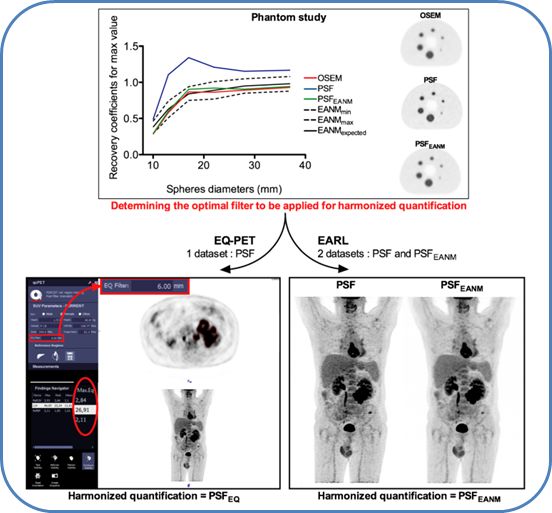
软件方案与二次重建方案对比
大量的研究和实践也证实了EQ.PET——SUV均一化软件方案的应用,在PERCIST、EORTC [6]、Deauville评分[7]、患者良恶性分层[8]、多中心研究[9]等多种应用场景都有着非常优异的表现。因此,我们有理由相信,借助软件方案的便利性,SUV定量分析作为临床诊断和疗效评估的黄金时代即将到来。
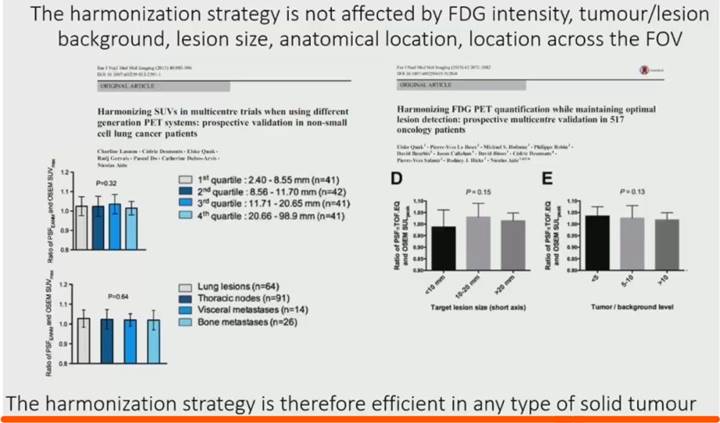
除了SUV以外,Aide教授还对肿瘤代谢体积(metabolic active tumor volume)的定量均一化进行了说明。同一病灶在不同的重建方法下获得的MATV不同,这是因为MATV的大小是根据SUV值计算的。因此,对SUV进行均一化的同时也将减少MATV的变异性。
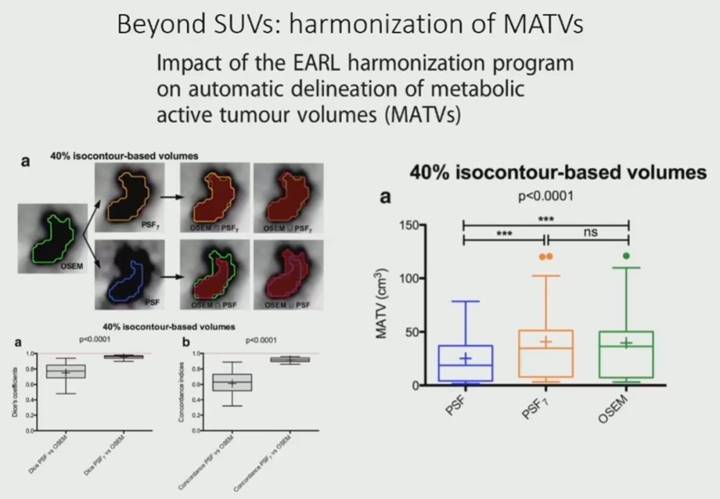
Summary
Nicolas Adie教授总结到:由于SUV的影响因素众多,其变异性一直是PET/CT临床中遇到的难题。EANM经过多年研究,提出进行两次重建图像的解决方案,这种方案虽然减少了SUV的变异性,但大大增加了临床工作负担。英国牛津大学和西门子经过多年研发,实现了一次重建就可同时获得最佳诊断效能的图像和均一化SUV值的方法:EQ.PET。经过多年的大量临床验证,EQ.PET受到EANM/EARL的认可并推荐在患者的疗效评估及随访监测中使用,尤其是那些有两台或多台不同机型PET/CT的科室。此外,在多中心临床实验中,EQ.PET可以使不同中心间的SUV值具有可比性。在计算肿瘤代谢体积MATV时,这种均一化方案也有效降低了测量值的变异性。

最后,我们来听听Nicolas Aide教授用法(fà)式英语介绍SUV均一化的解决方案和多场景应用的案例吧。
参考文献:
1. Young, H., et al., Measurement of clinical and subclinical tumour response using [18F]-fluorodeoxyglucose and positron emission tomography: review and 1999 EORTC recommendations. European Organization for Research and Treatment of Cancer (EORTC) PET Study Group. Eur J Cancer, 1999. 35(13): p. 1773-82.
2. Boellaard, R., Standards for PET image acquisition and quantitative data analysis. J Nucl Med, 2009. 50 Suppl 1: p.11S-20S.
3. Kaalep, A., et al., Quantitative implications of the updated EARL 2019 PET-CT performance standards. EJNMMI Phys, 2019. 6(1): p. 28.
4. Graham, M.M., et al., Summary of the UPICT Protocol for 18F-FDG PET/CT Imaging in Oncology Clinical Trials. J Nucl Med, 2015. 56(6): p. 955-61.
5. Lasnon, C., et al., Harmonizing SUVs in multicentre trials when using different generation PET systems: prospective validation in non-small cell lung cancer patients. Eur J Nucl Med Mol Imaging, 2013. 40(7): p. 985-96.
6. Aide, N., et al., EANM/EARL harmonization strategies in PET quantification: from daily practice to multicentre oncological studies. Eur J Nucl Med Mol Imaging, 2017. 44(Suppl 1):p. 17-31.
7. Quak, E., et al., The importance of harmonizing interim positron emission tomography in non-Hodgkin lymphoma: focuson the Deauville criteria. Haematologica, 2014. 99(6): p. e84-5.
8. Houdu, B., et al., Why harmonization is needed when using FDG PET/CT as a prognosticator: demonstration with EARL-compliant SUV as an independent prognostic factor in lung cancer. Eur JNucl Med Mol Imaging, 2019. 46(2): p. 421-428.
9. Quak, E., et al., Harmonizing FDG PET quantification while maintaining optimal lesion detection: prospective multicentre validation in 517 oncology patients. Eur J Nucl Med Mol Imaging,2015. 42(13): p. 2072-82.

更多精彩,欢迎点击关注哦