SUV 的由来
2020-12-24 来源:西门子
SUV 的由来
原创不想救公主的林克 MI V CLUB
上回说到PET/CT的历史,其实在PET和CT成为一家之前,就有许多研究者对PET定量进行了深度的思考。

picture source:musee rodin
早期核医学 定量初探MIVCLUB
收录于话题
1941年,当医生还在用32P治疗白血病患者的时候,为了获取组织内摄取的32P含量,医生会将不同组织的手术标本(取0.5mg)在500摄氏度的高温下进行焚烧,并用盖格计数器(Geiger counter)和劳里森验电器(Lauritsen electroscope)探测烧成灰(ash)的放射性活度。以此获得组织内32P的浓度(mCi/kg),如果将该浓度除以每公斤体重的32P注射剂量(mCi/kg),就得到了D.A.R.(differential absorption ratio),即组织对32P的吸收比值。[1]
DAR = tissue concentration(nCi/g) / (injected dose[nCi]/body weight[g])[2]

John Lawrence (right) was the first to use32P in treatment of leukemia.
picture source:A personal history of nuclear medicine
1980年代,当第一台PET诞生之后,最初的粗糙定量方式得到进一步优化,加入了多种校正方法,实现了根据PET图像像素(pixel)进行定量的方式。为了区别于之前使用的DAR,产生了DUR(differential uptake ratios)的概念:[3]

由公式可见,DUR实现了从counts向activity的转变。根据Dr. Cherry的论述,校正因子(calibration factor)由已知浓度的桶源经过PET扫描后,计算获得:[4]

PET图像上每个像素(pixel)内的计数(counts)除以校正因子CAL,就得到了像素内的单位计数(kBq/cm3),再乘以体素容积(voxel volume)就得到了体素内的放射性活度(kBq)。[4]

SUV 与 动力学分析
1990年代,随着FDG的广泛应用,越来越多的研究使用PET作为显像工具。为了统一组织对放射性示踪剂摄取比率的名称,标准化摄取值(standardized uptake value, SUV)应运而生,其定义与DAR和DUR颇为类似:

SUV计算的前提条件是:假设所有身体部位的密度都和水一样,即1mL=1g。这样一来,SUV公式上下的单位抵消,成为没有单位的一个比值,也被称为半定量参数(但素,Prof. Richard Whal不喜欢“半定量”这个说法)[5]。
与此同时,另一种绝对定量方法—动力学分析(kinetic analysis)—在FDG脑部研究中开展起来,研究者通过PET动态显像获得脑内FDG的绝对定量,即脑内不同组织对FDG的代谢率MRFDG(mol/100g/min)。MRFDG经过Lumped常数(LC)的换算,就可以得到相应组织的葡萄糖代谢率MRglu。葡萄糖代谢率可以更准确地反映真实的细胞糖代谢活动。[6]

1999年,当人们开始利用FDG PET进行疗效评估时,医生们试图找到一种最准确的定量方法,确保前后两次PET检查定量的一致性,从而准确判断肿瘤的变化趋势。当时,共有三种方法可进行疗效判断:[7]
· 目测法
· 测量标准摄取值(SUV)
· 动力学分析(kinetic analysis)
1999年,欧洲癌症治疗研究会(EORTC)在其发布的肿瘤疗效评估指南中对比了这三种方法的优缺点:[7]
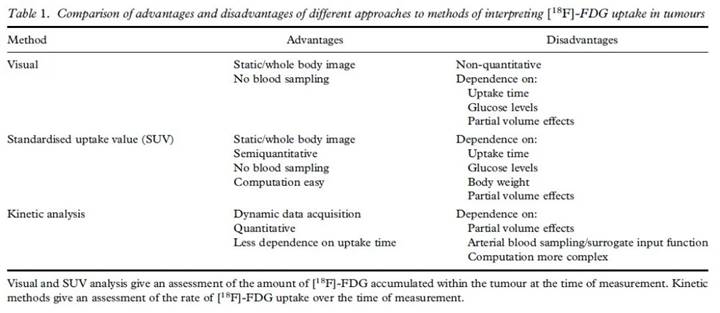
由于当时技术条件所限,动力学分析过于复杂,不适于广泛应用。视觉评估由于主观性太强、不能定量分析,也没有获得认可。SUV作为简便易行的定量方法,在临床中广泛开展起来。

SUV的困境 & 解决之道
随着SUV临床经验的增多,许多研究者发现SUV的影响因素远不止上表中列出的那几点,更有人因为SUV定量的差异性过大,称SUV为 “silly useless value”。[5]经过多年研究,SUV主要影响因素有以下几点:[8]
1. 患者因素:血糖水平、摄取时间、患者位移或呼吸、注射后休息环境、炎症反应等
2. 操作因素:PET与剂量计的校准、注射后针管内的剩余剂量、剂量计与PET扫描仪的时间校准、注射时间与测量活度时间的间隔、注射渗漏等
3. 物理因素:采集参数、图像重建参数、ROI大小、SUV归一化因子、血糖校准、CT造影剂的使用等
为此,欧洲核医学会(EANM)及北美核医学会(SNMMI)联合发布了《FDG PET/CT临床应用指南》,旨在形成规范化的扫描流程,尽可能减少因患者因素和技术操作因素引起的PET定量误差。[9]

但因为各个厂家或医院设置采集参数及图像重建参数的不同,SUV值仍然存在不可避免的误差。直到2015年EQ.PET的诞生,解决了由各厂家不同采集参数和重建参数引起的SUV值误差,实现不同设备之间SUV值的可比性。EQ.PET发布后经过大量的临床验证,最终受到欧洲核医学多中心研究协会(EARL)的认可和推广,为减少SUV定量误差更进一步。[10]


回顾历史,从1941年的DAR、1980年代的DUR到90年代的SUV,走过“silly useless value”的弯路...... 直到今天,SUV在许多方面得到了改善。但是,PET/CT定量的脚步没有停滞。随着科技的进步,人工智能的应用,PET将告别半定量的时代,迈入绝对定量的新世纪。
精益求精,为患者、更为未来的我 们 自 己。
参考文献:
1. Kenney,J.M., L. Marinelli, and H.Q. Woodard,Tracerstudies with radioactive phosphorus in malignant neoplastic disease.Radiology, 1941. 37(6): p. 683-690.
2. Woodard, H.Q., et al.,Expression of tissue isotope distribution.Journal of Nuclear Medicine, 1975. 16(10):p. 958-959.
3. Kubota, K., et al.,Lung tumor imaging by positron emissiontomography using C-11 L-methionine.Journal of nuclear medicine, 1985. 26(1): p. 37-42.
4. Cherry, S.R., J.A. Sorenson, andM.E. Phelps,Physics in nuclear medicinee-Book. 2012: Elsevier Health Sciences.
5. Wahl, R.L., H.N. Wagner, and R.S.Beanlands,Principles and practice of PETand PET/CT. 2009: Lippincott Williams & Wilkins Philadelphia, PA:.
6. Herholz, K., J. Rudolf, and W.-D.Heiss,FDG transport and phosphorylationin human gliomas measured with dynamic PET.Journal of neuro-oncology,1992. 12(2): p. 159-165.
7. Young, H., et al.,Measurement of clinical and subclinicaltumour response using [18F]-fluorodeoxyglucose and positron emissiontomography: review and 1999 EORTC recommendations.European journal ofcancer, 1999. 35(13): p. 1773-1782.
8. Boellaard, R.,Standards for PET image acquisition and quantitative data analysis.J Nucl Med, 2009. 50 Suppl 1: p.11S-20S.
9. Boellaard, R., et al.,FDG PET/CT: EANM procedure guidelines fortumour imaging: version 2.0.European journal of nuclear medicine andmolecular imaging, 2015. 42(2): p.328-354.
10. Aide, N., et al.,EANM/EARL harmonization strategies in PET quantification: from dailypractice to multicentre oncological studies.Eur J Nucl Med Mol Imaging,2017. 44(Suppl 1): p. 17-31.